共通テスト「化学」全問解説
2021年度(令和3年度)大学入学共通テスト 本試

どこよりも詳しく、わかりやすい過去問の分析と解説(解説動画付き)
第4問 有機化合物
第4問 問1 ベンゼン環の性質
このタイプの問題の正しい攻略法を身に付けましょう。
とりこぼすことなく、かつ、より速く解答できるようになります。
今回の解説でも何度か出てきましたが、このタイプの問題では、正解の選択肢が明らかなまちがいを含んでいるのがパターンです。
そして、その「明らか」は、思考力によって導かれる「明らか」です。
では、どのように「明らか」にまちがいなのか?みていきましょう。
選択肢①からです。
一般の解説では、ナフタレンをこの条件で反応させると生成するのは「無水フタル酸」だから、この選択肢がまちがい・・・と解説されています。
ご安心ください。・・・この程度のことで「明らか」というつもりは、ありません。
確かに、教科書でもフタル酸の製法としてナフタレンの酸化も少し紹介されていますが、それは覚えておかないといけないことでしょうか?
・・・私は、そうでもないと思います。
少なくとも、共通テストでそんな細かい知識を問われることはないと、断言できます。
では、なぜ「明らかに」ちがうと判断できるのか?(しかも、すぐに・・・)
選択肢①の文を、よく読んでみましょう
「高温で酸化バナジウム(Ⅴ)を触媒として酸素を反応させる」・・・とあります。
ふつうに考えて、「酸化させる」と考えていいでしょう。
重要な物質である「硫酸」の製法で、酸化バナジウム(Ⅴ)は二酸化硫黄SO₂ を三酸化硫黄SO₃ に酸化させるための触媒として出てきました。
ここでも、「ナフタレンを酸化させた」と、とらえていいでしょう。
ここで、o-キシレンの構造式をみてみましょう。(こういう問題では、ナフタレンやo-キシレンの構造式をかいてみて、それをみながら考えるくらいしましょうね。)

酸化されたはずなのに・・・
O(酸素原子)なんて・・・くっついていませんね。
ここで、「誤りを含む」と判断してもいいくらいですが、酸化される場合、H(水素原子)が減るかたちになることもあるので(問3aで出てきます)、一応、水素原子の数も確認しておきましょう。図をみて数えればいいです。
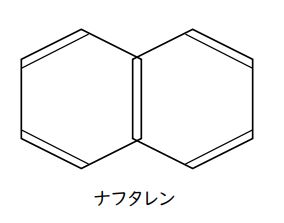
それぞれの化学式を確認すると・・・
ナフタレンC₁₀H₈ 、0-キシレンC₈H₁₀
・・・水素原子の数(割合)は、むしろ増えちゃっていますね。
ということで、ナフタレンが酸化されてo-キシレンになったということは、あり得ません。
・・・ここで、少しお待ちください。
私は上記の内容をていどで、「明らかに」誤り・・・と言っているわけではありません。
ここからが本題です。
もっとも、この時点で正解は①と判断できるので次に進んでもいいですが、化学の基礎力を底上げするためにも、以下の内容もおさえておくとよいです。
有機化合物なら有機化合物の単元で、さまざまな反応や現象を理解するために、おさえておくべきポイントがあります。
その中でも、大きなもののうちの1つが、次のようなものです。
「ベンゼン環に結合している炭化水素基は、KMnO₄ などの酸化剤によって、その炭素数にかかわらず、カルボキシ基-COOH 『まで』酸化される」
もっと簡単にまとめてもいいです。
「ベンゼン環に結合している炭化水素基は、簡単に酸化されてカルボキシ基-COOH になる。」
「ベンゼン環に結合する炭化水素基」とは、まさにo-キシレンの-CH₃ などのことです。
問題にもどりましょう。
選択肢①を読んで、ナフタレンとo-キシレンの構造式をかいてみて・・・形としては似てますからね・・・そういうふうに変化することもあるかもしれない・・・と思ってしまっても、それは仕方のないことです。
でも、上記の「ベンゼン環に結合している炭化水素基は酸化されやすい」というポイントがしっかり入っていれば、「おかしいな?」と思えるはずですし、思えないといけません。
o-キシレンは、「酸化されてできるもの」ではなく、「(これから)酸化されやすいもの」です。
実際、o-キシレンは過マンガン酸カリウムKMnO₄ などの酸化剤によってフタル酸になります。
これは、覚えていかないといけないこと・・・というよりは、上記のことから、すぐに自分で導けないといけないことです。(反応式は、下にまとめて画像を貼っておきます。)
まとめます。
これから説明するのが、選択肢①が明らかに誤りを含むと判断できる根拠です。
選択肢①の文は、「高温」「酸化バナジウム(Ⅴ)を触媒」など、(単に過マンガン酸カリウムを加えるのに比べても)一生けん命、酸素と反応させよう(酸化させよう)としていますね。
酸化されやすい(といってもよい)o-キシレンの形のまま、反応がストップするということは、考えられません。
ということで、選択肢①が、明らかにあやまりです。
出題者側も、このように考えてこの選択肢を選ぶことを想定していると思います。
なお、ここまで書きましたが、フタル酸の製法として「ナフタレンやo-キシレンの酸化」がしっかり入っていて、それをもとに答えられれば、それならそれにこしたことはありません。
私としては、上記のように考えていく過程で、「o-キシレン→フタル酸」の反応を確認した時点で、「そういえば、ナフタレンからも無水フタル酸をはさんでフタル酸ができるなんて話があったな・・・」と思い出せるくらいでちょうどいいだろうと考えます。
(参考図)

正解:①
他の選択肢も一通り確認しておきましょう。
すべて、基本的なベンゼンの反応です。(下に画像でまとめておきます。)
ベンゼン環の六角形には便宜的に二重結合がかかれますが、これは鎖式の炭化水素の二重結合とは別のもので、単結合と二重結合の中間のような性質を持ちます。
鎖式炭化水素の二重結合には付加反応が起こりやすかったですが、ベンゼンの二重結合はそれより安定なので、付加反応は起こりにくいです。
その代わり、ベンゼンの-Hと、他の原子または原子団といれかわる置換反応が起こりやすいです。
選択肢②と③が、ベンゼンの置換反応としてよくあげられる例です。
選択肢②:ハロゲン化
・・・ベンゼンに鉄または塩化鉄(Ⅲ)を触媒として塩素Cl₂ を反応させると、クロロベンゼンが生成します(下図参照)。同じくハロゲンである臭素Br₂ も同様の反応をします。
選択肢③:スルホン化
・・・強酸であるベンゼンスルホン酸を生成する反応です。
注目すべきところは濃硫酸を、高温で反応させる(加熱する)というところです。
「熱濃硫酸」による脱水作用を利用した反応です(下図参照)。
一方、特別な触媒を使うなどかなり厳しい条件で行えば、ベンゼンにも付加反応が起こります。
選択肢④が、その例です。「高温・高圧」でニッケルを触媒として水素を反応させるとシクロヘキサンが生成します(下図参照)。

第4問 問2 乾性油の性質
選択肢①の解説のため、説明の効率から先に選択肢④を確認します。
この記述は、正しいです。そもそもの話です。高級脂肪酸とグリセリンのエステルが油脂です。
下線部に含まれる(1,2,3-プロパントリオール)の別称が気になるかもしれませんが、大丈夫です。
今回の解説でも何度か出てきましたが、このタイプの問題で誤りを含む正解の選択肢は、明らかな誤りを含んでいるものなので、こういうところが正解になることはありません。
それでは選択肢①から、みていきましょう。
なお、「下線部に誤りを含むもの」選べという指定なので、下線部以外のところには正しいことが書かれているということです。それをふまえて、その場でしっかり考えながら判断していきましょう。
選択肢①:カルボン酸である高級脂肪酸と、アルコールであるグリセリンをむすび付ける反応がエステル化です。
けん化は、いわばその逆の反応で、塩基でエステルを加水分解し、アルコールとカルボン酸の塩に分解する反応です(セッケンの製法でもありますね)。
けん化価の説明は、選択肢の文のとおりです。
油脂は1gと固定されています。
もし、この油脂の分子量が小さければこの1gの中に多くの油脂分子があることになり、分子量が大きければ油脂分子の数は少ないことになります。
1つの分子の中に含まれるエステルの数は決まっています(3つです)。
また、1gの油脂に含まれるエステルの数が多いほど、けん化するのに必要な水酸化カリウムの質量(けん化価)は、大きくなります。
「けん化価が大きい」→「1gの油脂の中にたくさんのエステルがある」→「油脂分子がたくさんある」→「1分子あたりの分子量(平均分子量)は小さい」
この選択肢は正しいです。
選択肢②、③に関しましては、油脂についての分類ができていないと意味が分からないでしょうから、先に簡単に確認しておきます。
油脂は、常温で液体である「脂肪油」と、常温で固体である「脂肪」に分類されます。
(漢字では「あぶら」は、液体のものを「油〔あぶら〕」、固体のものを「脂〔あぶら〕」と表記します。合わせて「油脂」です。)

常温での状態にちがいが出るのは、それぞれの油脂を構成する脂肪酸の種類によります。
脂肪は、「飽和脂肪酸(飽和結合〔単結合〕のみをもつ脂肪酸)」を多く含みます。
一方、脂肪油は「不飽和脂肪酸(不飽和結合〔二重結合など〕をもつ脂肪酸)」を多く含みます。
飽和結合(単結合)の部分は、分子が直線状になります。よって、飽和脂肪酸を多く持つ脂肪は、分子どうしが近づきやすく分子間力が強くなり、常温で固体になります。
一方、不飽和結合(C=C)の部分では分子が折れ曲がっているので、分子どうしが近づきにくくなります。
したがって、不飽和脂肪酸を多く含む脂肪油は、分子間力が弱くなり、常温で液体になります。
ここまで、いいでしょうか?
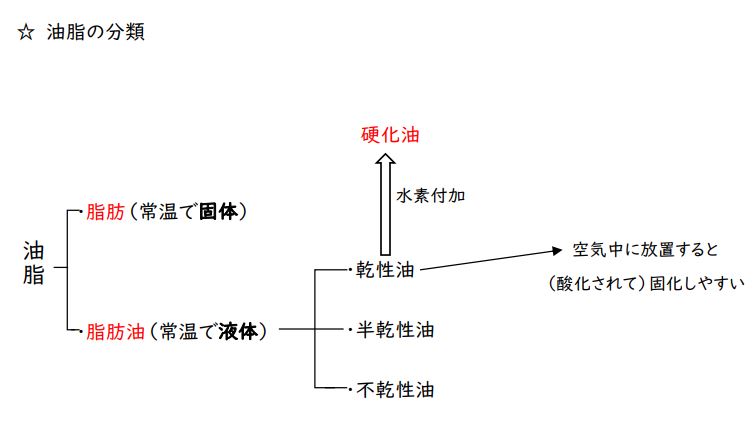
まず油脂が、脂肪と脂肪油の2つに大きく分類されました。
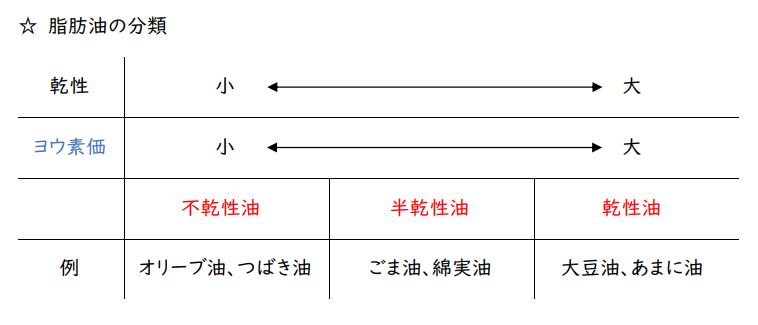
さらに、「脂肪油」は不飽和結合が含まれる度合いにより、乾性油・半乾性油・不乾性油に分類されます。
その「不飽和結合が含まれる度合い」を調べるのが、選択肢②に出てくる「ヨウ素価」です。
選択肢②:ヨウ素化の説明は、選択肢の文のとおりです。
炭素原子間の二重結合(C=C)にヨウ素I₂は付加し、ヨウ素の色が消えますので、一定量の油脂にどれだけのヨウ素が付加するのかを調べることができます。
「ヨウ素価が大き」ければ、「C=C結合の数が多く」、その油脂は「不飽和脂肪酸を多く含む」ということができます。
設問文も注意深く読みましょう。
「空気中で放置する」・・・とは、どういうことでしょうか?
・・・そうです。「酸化してしまう」ということですね。
酸素原子は、中学校のときのいい方ですが「手を2本」持っていますね。
一方、不飽和脂肪酸を多く含む油脂は、他のものと結びつきやすい二重結合を多く持っています。
脂肪酸の分子どうしが O(酸素原子)によって橋渡しされて結び付き、分子量が大きくなり、かたまります。(分子量が大きいほど、分子間力も大きくなり融点が高くなるのは基本です。)
ヨウ素価が大きい方が、不飽和度が高く固化しやすい乾性油ということでまちがいないので、この選択肢は正しいです。この空気中で固まりやすいという性質は、油絵具やペンキ塗装が乾くのを思い浮かべればよいでしょう。
なお、飽和脂肪酸や不飽和度が低い脂肪酸を多く含む油脂は不乾性油といい、ヨウ素価は低いです。
また、乾性油と不乾性油の中間の不飽和度(ヨウ素価)を持つ油脂を半乾性油といいます。
選択肢③:選択肢②と対で「乾性油の乾燥」と「硬化油」の区別がついているかを問う問題でした。
硬化油は、主として乾性油からつくられます。
分子の大きさに加え、油脂や脂肪酸においては、不飽和度も融点に大きく関わってきます。
同一炭素数での融点は「(不飽和脂肪酸)<(飽和脂肪酸)」となります。
(C=C結合(シス型)があると、分子の形が屈曲し、分子どうしが近づきにくくなり、分子間力が弱くなる・・・ということです。)
不飽和度の高い液体状の油脂に、水素を付加させることによって、不飽和度がひくくなり、 融点が高くなり常温で固体になります。
こうしてできるのが、硬化油です。選択肢③が誤りを含む正解の選択肢です。
なお、
液体状の植物油脂に水素付加 ⇒ マーガリン(の原料)
・・・は、IOPでもあります。
でも、この問題のポイントは、選択肢②が「酸化しちゃう」と読み取れるかどうかですね。
そうすると、③も「酸化」なので、②と③のどちらかが誤りだと判断できます。
また、マーガリンをつくるときにはニッケルを触媒として高温で水素を付加させます。
特別な操作をしているということですね。
「酸化しちゃう」と「(特別な操作をして)水素を付加させる」の区別の問題だともいえます。
正解:③
第4問 問3a アルコールの酸化
アルコールの酸化に関する問題です。
まず、アルコールはヒドロキシ基-OHに結合する炭素の状態により分類できました。
その炭素原子に、他の炭素原子が何個結合しているかで、第一級アルコール、第二級アルコール、第三級アルコールと分類できます。
「一」、「二」、「三」という数は、-OHに結合したCに、結合しているCの数、・・・と考えてもいいでしょう(下図参照)。
「酸化される」という場合、酸素原子(O)と結びつく変化だけではなく、水素原子(H)が奪われる形で、酸化されることもあります。

「第一級アルコール」は、酸化されてH原子を2個失い「アルデヒド」に、さらに酸化されて「カルボン酸」にまで変化します。
「第二級アルコール」は、酸化されてH原子を2個失い「ケトン」に変化し、それ以上は反応しません。
第一級アルコール、第二級アルコールとも、H原子を2個(-OHのHと、-OHが結びついているCに結びついているH)失い、そのような形になることを、上図をみて確認しましょう。
「第三級アルコール」が、酸化されようもなく反応しないことも、理解できるはずです。
「第一」「第二」「第三」などの名称よりも、まずこのしくみを理解しましょう。
問題に入ります。第二級アルコールを選べばよい問題です。
でも、第二級アルコールを選ぶというよりも、酸化されて(H原子が2個取れて)どうなるか?・・・と思ってみていった方が、考えやすいでしょう。
パズル遊びみたいなものです。そう思えるようになりましょうね。
くり返しますが、H原子2個とは「-OHのHと、-OHが結びついているCに結びついているH」のことです。
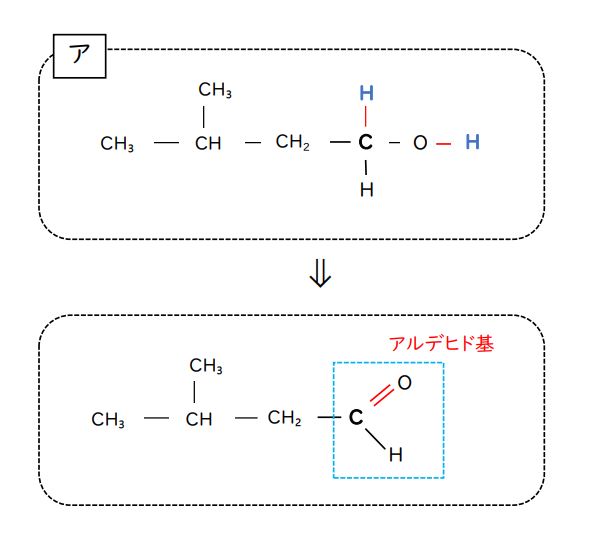
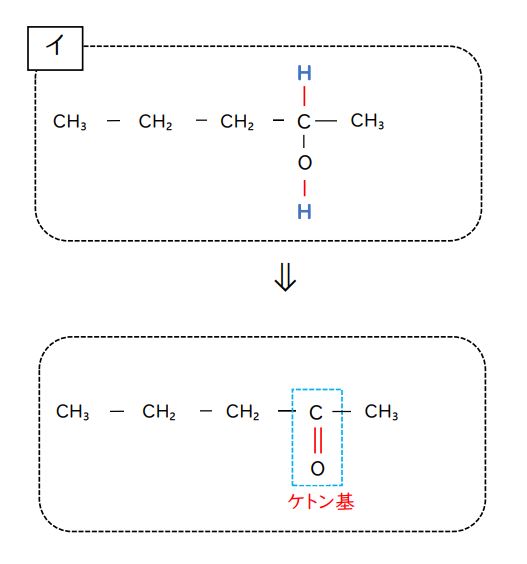
アからはアルデヒド基ができることがわかりますね。イ、ウ、エからは、ケトン基ができます。答えは3つです。アルデヒド基を持っている物質の総称がアルデヒド、ケトン基を持っている物質の総称がケトンです。
(下に参考図をのせておきますが、自分でノートなどにどうなるか?をかいてみてから確認するようにしましょう。)
正解:③
(参考図)


第4問 問3b アルケンの異性体
パズル遊びみたいなものです。そう思えるようになりましょうね。
問題文を、よく確認しましょう。
OH基の結合した炭素原子からOH基がとれ、その炭素原子の隣の炭素原子からH原子がとれて、アルケンが生成します。(これらの炭素原子は、下図では青色で示しました。)
「隣」といっても「左隣」と「右隣」の場合があり、それがこの問題のポイントです。
なお、図ではわかりやすいように、これらの炭素原子に限り、結びついている水素原子のようすがわかる構造式にしました。
アルケンになったとき二重結合になる価標(かひょう)は赤線で示しました。
OH基とH原子が、もとのアルカンから離れていくとき・・・
OHに結びついていた価標と、H原子が結びついていた価標とが結びつき、二重結合になるということを、自分でも図をかいてみて、感覚をつかんでおきましょう。
本番のテストのときも、空白や下書き用紙は十分に与えられているので、こういう問題は、せいせい書き出してみた方が速いです。
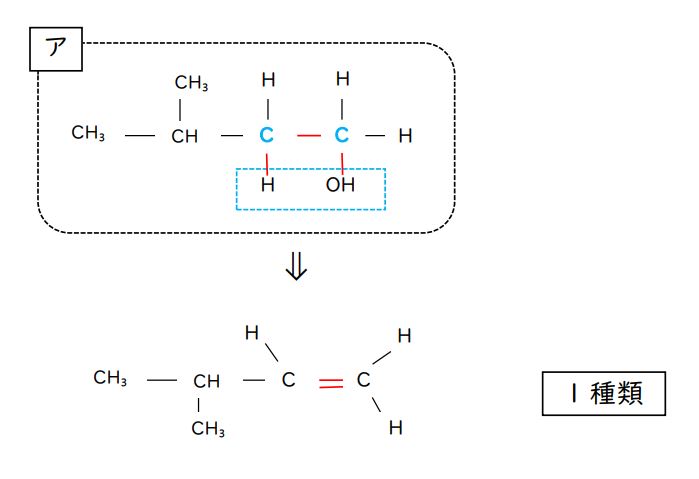
ア:この場合、「OH基の結合した炭素原子の隣の炭素原子」は1個ですので、生成するアルケンも1種類です。
また、上図で二重結合をつくる右側の炭素原子に結びついているのは、2つともH原子ですので、シス―トランス異性体は生じません。(二重結合をつくる左側の炭素原子に結びついている原子(原子団)を上下入れ換えたとしても、分子全体をひっくり返せば、同じ形です。)
アから生成するアルケンは「1種類」です。

イ:「OH基の結合した炭素原子の隣の炭素原子」というのが、「左隣」のものである場合と「右隣」のものである場合があります。図やここでは、〔左〕〔右〕と表します。
〔左〕:二重結合をつくる2つの炭素原子に、それぞれ別の2つの原子団(原子)が結びついています。
このような形のとき、シス―トランス異性体(幾何異性体)が存在します。
(上図では、二重結合をつくる炭素原子の、どちらも上側に水素基-Hがついているのでシス型です。どちらか片方の炭素原子だけ、上下の-H と、-CH₃ または-CH₂-CH₃ とが入れ替わったら、トランス型です。)
イ〔左〕から、2種類の異性体が生成します。
〔右〕:シス―トランス異性体が存在しない形です。こちらから生成するアルケンは、1種類です。
以上より、〔左〕と〔右〕から、選択肢イのアルコールからは、2+1=3より、計「3種類」の異性体が生成します。
問題の内容も、みえてきました。
各選択肢、〔左〕と〔右〕の2つがあり、それぞれにシス―トランス異性体があるので、最大で、2×2=4より、4種類の異性体が生成する可能性があります。
「3種類」の選択肢イは、正解の候補となりそうです。
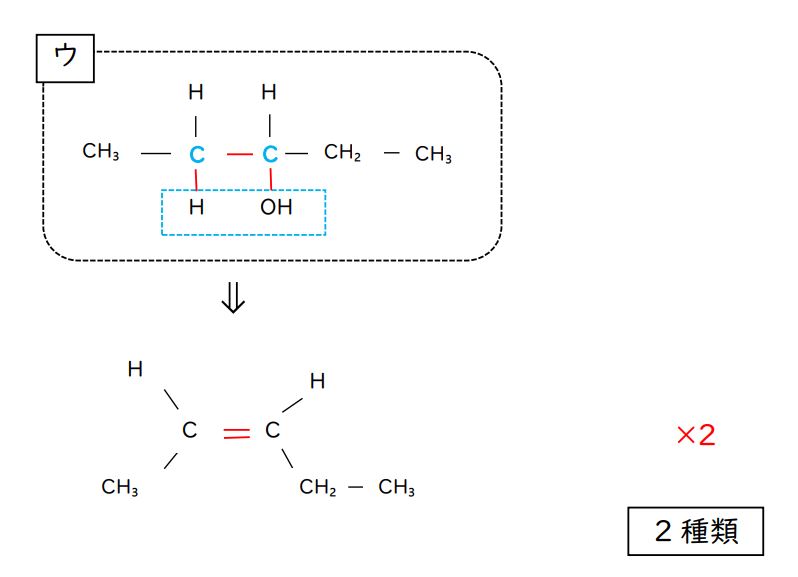
ウ:この選択肢もポイントです。
OH基の結合した炭素原子は、ちょうど中央に位置しますので、「左隣」も「右隣」も同じです。
ひっくり返せば、同じ形になります。
この時点で、生成するアルケンの数は最大で2種類なので、この選択肢は切ってもよいですが、一応確認してみましょう。
上図のように、シス―トランス異性体が存在する形なので、選択肢ウから生成する異性体の数は「2種類」です。
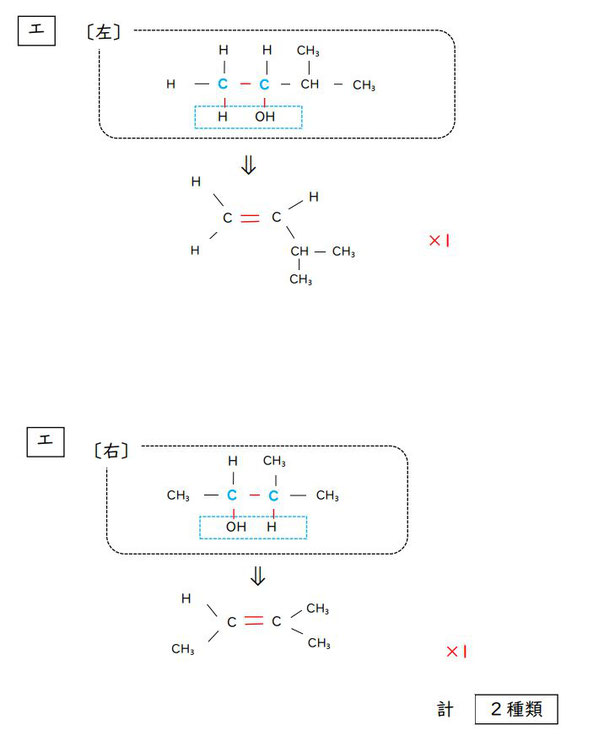
エ:選択肢の中では、形が複雑な方ですね。
ですから、異性体も2×2のフルに存在して4種類・・・ということで、この選択肢が答えになるか?
それとも、案外、異性体の数は少なく選択肢イの方が答えになるか?
・・・そういう問題です。(そういう問題なんですよ。私は、後者を予想しました。)
それでは、〔左〕からみていきましょう。
〔左〕:上図参照。さっそく、シス―トランス異性体が存在しない構造です。
こちらからは、1種類のアルケンが生成します。
〔右〕:こちらも、二重結合をつくる炭素原子のうち右側のものに、上下とも-CH₃ と、同じ原子団がくっついている形になりました。こちらにも、シス―トランス異性体は存在しません。
こちらから生成するアルケンも1種類です。
ということで、選択肢エから生成する異性体の数は(予想通り思ったより少なめで)「2種類」です。
選択肢イが、正解でした。
正解:②
第4問 問4 高分子化合物
①:「ナイロン66(ろくろく)」や「ナイロン6」の、「66」や「6」が何を意味しているか?
・・・これが、この選択肢どころか、この問題のポイントとなります。
これも、ナイロン66やナイロン6が、どのようにできているか?たとえ、記憶があいまいだったとしても、「66」と「6」が意味している内容から、正解にたどりつくことができます。(一応、図は示しますが、それを完璧に覚えてなくても、正解は出せるという意味です。ただし、これは、覚えておいた方がいいですけどね。)
まず、アミド結合について確認しておきましょう。
アミノ基(-NH₂)のHと、カルボキシ基(-COOH)のOHと、水分子1個分が奪われて縮合した(脱水縮合)形の「-NH-CO-」という結合を、アミド結合といいます(下図参照)。
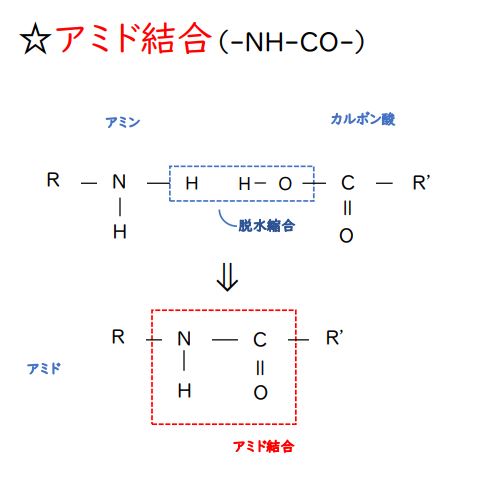
合成高分子化合物は、低分子化合物の単量体(モノマー)が重合して生成されます。
重合の際、単量体どうしが結びつきますが、アミド結合で結び付くものもあり、ナイロン66とナイロン6が、それにあたります。
アミド結合は、タンパク質に多く含まれる結合であり、ナイロン66やナイロン6もアミド結合を多く含むので、絹のような感触を持ちます。そのため、女性用のストッキングなど、幅広く利用されています。
ナイロン66の原料は、「アジピン酸 HOOC-(CH₂)₄-COOH」と「ヘキサメチレンジアミン H₂N-(CH₂)₆-NH₂」であり、両方とも炭素原子を6こ持つ化合物なので、ナイロン66という名前がついています。
アジピン酸は両端にカルボキシ基 -COOH、ヘキサメチレンジアミンは両端にアミノ基 -NH₂ を持ち、これらが脱水縮合してアミド結合を形成し、ナイロン66の構成単位(繰り返し単位)になります。
ナイロン66は繰り返し単位の中に、すでにアミド結合を一つもっているということになります。
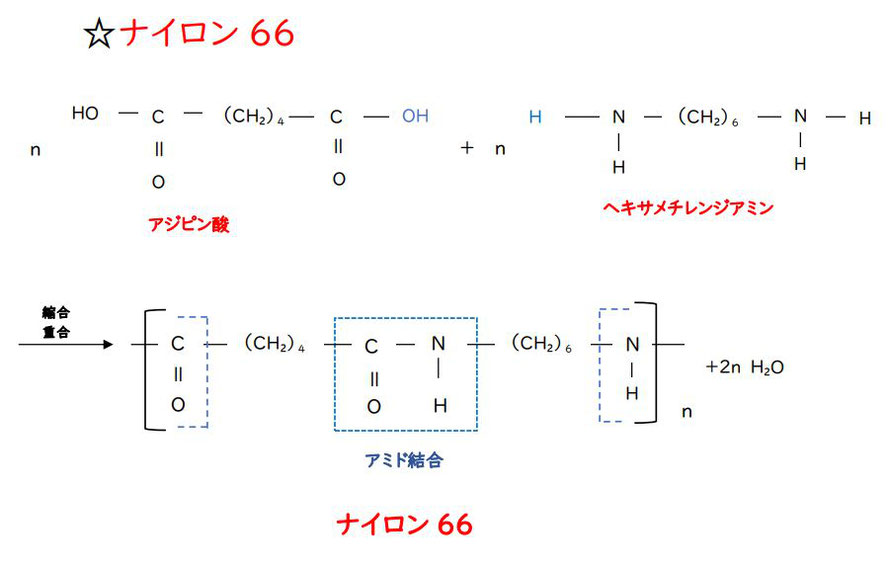
また重合する際、この繰り返し単位は、また別の繰り返し単位とアミド結合で結合していきます。
上図でいうと、左端の-CO は別の分子の-NH と結合し、右端の-NH は別の分子の-CO と結合していきます。
この、左端の-CO と右端の-NH で、アミド結合一つ分です。
よって、ナイロン66は構成単位(繰り返し単位)の中にアミド結合を二つもっています。
一方、ナイロン6はカプロラクタム(炭素原子数6)の開環重合によって、つくられます。
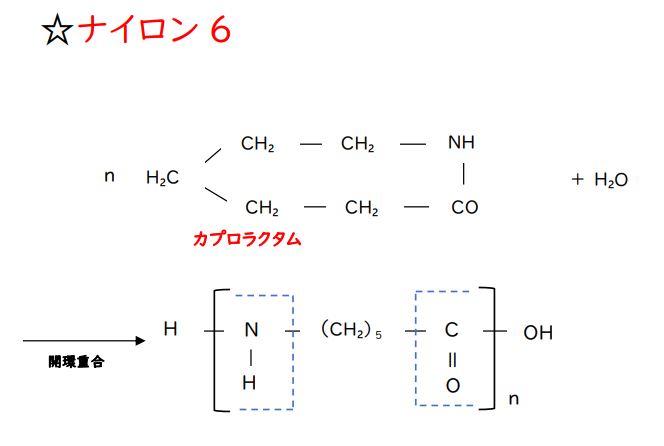
加水分解によって、環が開かれ両端にカルボキシ基-COOH とアミノ基-NH₂ ができ、それらにより付加重合してくと考えればいいでしょう。
こちらの構成単位も、左端の-NH と右端のの-CO で、アミド結合一つ分持っていることになります。
冒頭で、「これらの分子の形の記憶があいまいだったとしても、正解は出せる」という話をしました。
今から、それを説明します。
アミド結合により、重合体(ポリマー)がつくられるとすると、単量体どうしが結合するために両端にアミド結合一つ分、もつことになります。
選択肢①の文のように、「繰り返し単位の中にアミド結合を二つもつ」ためには、その繰り返し単位の(両端ではなく)内部にもアミド結合が一つある必要があります。
ナイロン66は、「66」という名前のように繰り返し単位の中に2種類の分子があり、その2種類の分子はアミド結合で結び付いている可能性もありますよね(実際にそうです)。
一方、ナイロン6は、ナイロン66に対して「6」という名前から、繰り返し単位の中に分子は1種類しか持っていないことがわかります。内部にアミド結合をもつことは、少し考えづらいですね。もしもっているとしたら、ナイロン66のように炭素原子の数をならべた名称になっているはずです。
もちろん、ナイロン66やナイロン6の構造がしっかり入っていれば、それにこしたことはありません。
どちらにせよ、この選択肢はナイロン66との混同を想定した選択肢だろうと、最初に予想できるといいですね。
この選択肢が、明らかに誤りを含みます。
正解:①
他の選択肢も、簡単に確認していきます。
選択肢②:日本でつくられた最初の合成繊維であるビニロンの製法の一部です。
作業着やロープなどに利用される、有用な合成繊維でありますので、その製法はしっかりおさえておきましょう。
きりがないので、ここではくわしく説明しませんが、要点だけいうと・・・
ビニルアルコールは不安定なので、ビニルアルコールから直接ポリビニルアルコールはつくれません。
そこで、酢酸ビニルからポリ酢酸ビニルをつくり、選択肢②の文にあるように、ポリ酢酸ビニルを加水分解してビニロンの原料であるポリビニルアルコールをつくります。
選択肢③:尿素樹脂は、熱硬化性樹脂です。
ボタンやコンセントの材料などに使われています。
熱可塑性樹脂に比べて、熱硬化性樹脂の方が数が限られているので、熱硬化性樹脂の方をおさえて、それ以外はすべて熱可塑性樹脂だと考えてよいです。
選択肢④:この操作を加硫(かりゅう)といいます。
選択肢⑤:ポリエチレンテレフタラート・・・PETのことです。
丈夫でしわになりにくく乾きやすいので、Yシャツやスーツなどに利用されている合成繊維です。
また、PETボトルでおなじみのように合成樹脂としても用いられています。
この場合は、PETは、服にも容器にも用いられているから、この選択肢は正しい・・・と判断すればよいでしょう。
第4問 問5 ポリペプチド鎖のらせん構造の全長の導出
センター試験とは大問の数とか構成が少しちがいますが、センター試験でいうとこのポジションにきていた問題は・・・
「一見、ものすごく難しそうだけど、解いてみるとビックリするほど簡単」・・・という問題です。
本当ですよ。きっと、ここまでさんざん頭を使って疲れているだろうから、取り組みさえすれば軽くとれる問題を入れておいてやろう、という出題者側の配慮だと思います。
共通テストに代わったので、どうなるかはわかりませんが、そういう仮定で進めましょう。
実際、化学の計算問題では、・・・
「なるべく頭を使わないですむ方法を考える」方針・・・が、正しいです。
(確実性という観点から、その通りです。)
それをふまえて、問題をみていきましょう。
このポリペプチド鎖は、アミノ酸Bのみを脱水縮合して合成されたものだそうです。
アミノ酸は、1分子中カルボキシ基-COOH とアミノ基-NH₂ をもち、前問でみたように水分子1つ分がとれ、アミド結合によりつながっていきます。(アミノ酸どうしが結合してできたアミド結合は、特にペプチド結合といいます。)
アミノ酸Bの分子量が与えられていますが、アミノ酸1分子から水1分子分(分子量:18)がとれて結合していくので、89-18=71から、この「71」という数字を使って、考えていく必要があります。
設問文に合わせてこの「71」を「アミノ酸の単位」の式量と呼ぶことにします。
とりあえず、このポリペプチド鎖がいくつのアミノ酸Bからできているのか?を考えてみましょう。
ポリペプチド鎖の分子量2.56×10⁴のなかに、脱水したアミノ酸単位の式量71がいくつ入っているかを調べればよく、わり算で・・・
2.56×10⁴÷71・・・
・・・やめておきましょう。すぱっとわれません。
そんな難しいはずが、ありません。(私が最初にこのテストをざっと一通り解いてみたとき、実際このように心が動きました。)
なら、「ひと巻分の式量」を最初に出しておこう・・・という発想になりますね。
アミノ酸の単位の式量71に、ひと巻分の個数3.6をかければよく、
71×3.6=255.6・・・きましたね。
有効数字3桁でとって、「256」・・・これが、アミノ酸「ひと巻分の式量」です。
これからの計算は簡単です。
ポリペプチド鎖の分子量が2.56×10⁴・・・10⁴は2.56にかけてしまいましょう。
小数点4粒の沖くして、ポリペプチド鎖の分子量は「25600」です。
「ひと巻分の式量」は「256」でした。
よって、このポリペプチド鎖が何巻でできているかは、25600の中に256がいくつ含まれていれば考えればよく、わり算で(暗算で十分ですね)、・・・
25600÷256=100・・・「100巻」です。
ひと巻分の間隔が0.54nm です。これが100巻あるので、かけ算で(もちろん暗算)・・・
0.54×100=54・・・54nm とわかりました。
やってみさえすれば、びっくりするほど簡単・・・というのが、お分かりいただけたでしょうか。
正解:②
以上です。ありがとうございました。
コメントなどいただけると、とてもうれしいです。
執筆:井出進学塾(富士宮教材開発) 代表 井出真歩
お問い合わせ
電話番号
0544-54-3412
受付時間:午前9時~午後10時(毎日、授業しております。)
ホームページをみた、と言ってください。
井出進学塾
富士宮市上井出344-1
井出進学塾 (木曜日, 11 1月 2024 12:10)
to たな さん
ありがとうございます。
実は、そここそ注力しているというか、自信があるところなので、そこにふれていただいてうれしいです。
たな (水曜日, 10 1月 2024 20:04)
出題意図まで踏まえて解説しておられる方はなかなかいらっしゃらないので、大変助かります。
井出進学塾 (水曜日, 21 12月 2022 13:34)
to コウ さん
ありがとうございます。
受験生の方でしょうか?
共通テスト、がんばってくださいね。
コウ (火曜日, 20 12月 2022 23:10)
先生の解説が面白くて、本当にわかりやすかったです!!